Le traitement par CAR-T cells (Chimeric Antigen Receptor T cells) est fondé sur une technologie ayant recours aux propres cellules immunitaires du patient génétiquement modifiées pour détruire des cellules tumorales. Il s’agit d’une nouvelle approche thérapeutique porteuse d’espoir pour lutter contre les formes sévères de certains cancers du sang.
Parcours de soins – Fiches de consensus régionales lymphomes
Un groupe de travail régional a réalisé des fiches de consensus lymphomes destinées à faciliter la liaison entre les centres où sont administrés les CAR-T cells et les centres périphériques qui adressent les patients.
En savoir plus sur le groupe de travail régional
En 2023, les oncohématologues des centres qualifiés CAR-T cells des CHU de Bordeaux, Limoges et Poitiers ont élaboré des fiches de consensus lymphomes destinées à faciliter la liaison entre leurs centres où sont administrés les CAR-T cells et les centres périphériques qui adressent les patients au sein de la Nouvelle-Aquitaine.
L’objectif de ces fiches est d’harmoniser les pratiques au niveau régional et de guider les centres périphériques dans une prise en charge appropriée des patients atteints de lymphomes et bénéficiant des CAR-T cells aux différentes étapes du parcours de soins.
Ces fiches de consensus identifient le centre prenant en charge le patient à chaque étape de son parcours de soins et les informations indispensables à échanger entre centre qualifié et centre périphérique tout au long du traitement par CAR-T cells.
Fiches accompagnées des annexes qui représentent la base de travail (recommandations usuelles qui ont permis leur élaboration)
Fiches incluant une synthèse du suivi et un compte rendu type avec les informations à transmettre par les centres périphériques à leurs centres qualifiés pour le suivi de leurs patient
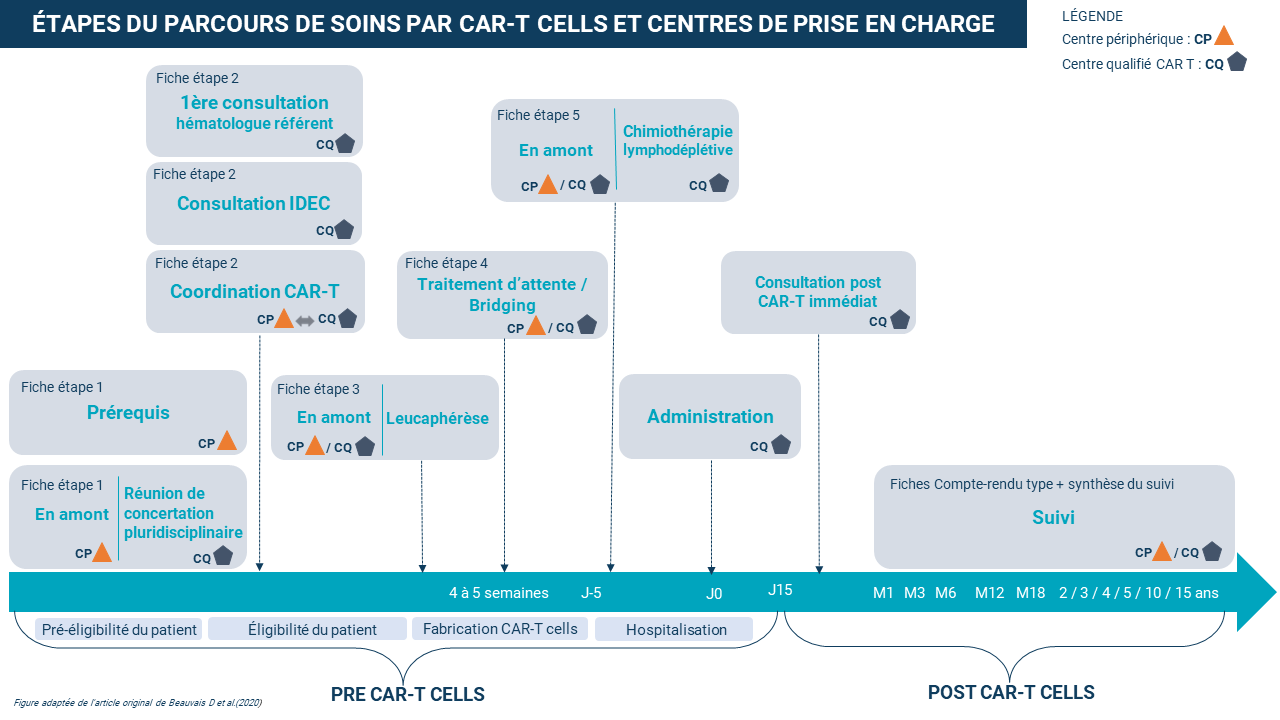
Télécharger les fiches de consensus par étape clé du parcours de soins par CAR-T cells
- Le parcours de soins du patient dans le cadre des CAR T-cell : recommandations de la Société francophone de greffe de moelle et de thérapie cellulaire (SFGM-TC). Beauvais D et al. Bull Cancer ; vol 107 : S170-S177 ; 2020. > Télécharger l’article (PDF)
- Éligibilité des patients aux cellules CAR-T : avis d’experts proposé par la SFGM-TC Beauvais D et al. Bull Cancer ; vol 108 : 725-729 ; 2021. > Accéder à l’article
- CAR-HEMATOTOX: a model for CAR T-cell–related hematologic toxicity in relapsed/refractory large B-cell lymphoma. Rejeski K et al. Blood ; vol 138 : 2499–2513 ; 2021. > Accéder à l’article
- Immune effector cell-associated hematotoxicity: EHA/EBMT consensus grading and best practice recommendations. Rejeski K et al. Blood ; vol 142 : 865-877 ; 2023. > Accéder à l’article
- How to perform leukapheresis for procurement of the staring material used for commercial CAR T-cell manufacturing: A consensus from experts convened by the SFGM-TC]. Carnoy S et al. Bull Cancer ; vol 108 : 295-303 ; 2021. > Accéder à l’article
- Management of adults and children receiving CAR T-cell therapy: 2021 best practice recommendations of the European Society for Blood and Marrow Transplantation (EBMT) and the Joint Accreditation Committee of ISCT and EBMT (JACIE) and the European Haematology Association (EHA). Hayden PJ et al. Ann Oncology ; 33 : 259-275 ; 2022. > Accéder à l’article
Recommandations nationales
La mise en œuvre du traitement par CAR-T cells nécessite une coordination multidisciplinaire et un encadrement strict.
Les avancées dans ce domaine soulèvent de nombreuses questions d’ordre éthique, pratique et juridique.
La législation française limite l’utilisation des CAR-T cells autologues à certains établissements de santé. Le traitement doit se faire dans un centre qualifié, autorisé à prélever les lymphocytes T et à administrer les cellules CAR-T
> Accéder à l’arrêté du 28 juin 2024 (mise à jour régulière sur le site Légifrance)
> Accéder aux centres qualifiés CAR-T
En 2019, la HAS a annoncé qu’elle réévaluerait les CAR-T cells afin de vérifier leur efficacité, tolérance ainsi que leur impact sur la qualité de vie à moyen et à long terme. Pour cela, elle a demandé à ce que des données complémentaires lui soient fournies annuellement. Ces données en vie réelle alimentent un registre commun aux différents CAR-T cells, le registre DESCART.
> Consulter le communiqué de presse de la HAS
La Société francophone de greffe de moelle et de thérapie cellulaire (SFGM-TC) travaille à :
- l’élaboration de procédures thérapeutiques partagées et harmonisées pour améliorer la sécurité et la qualité des soins des patients traités par CAR-T cells
- l’organisation d’ateliers d’harmonisation des pratiques , conduisant à des recommandations qui ont donné lieu à publications
Ces recommandations sont adaptées dans chaque centre en fonction de leurs moyens matériels et des ressources humaines.
> Accéder aux ateliers d’harmonisation des traitements par cellules CAR-T
Qu’est-ce que les CAR-T cells ?
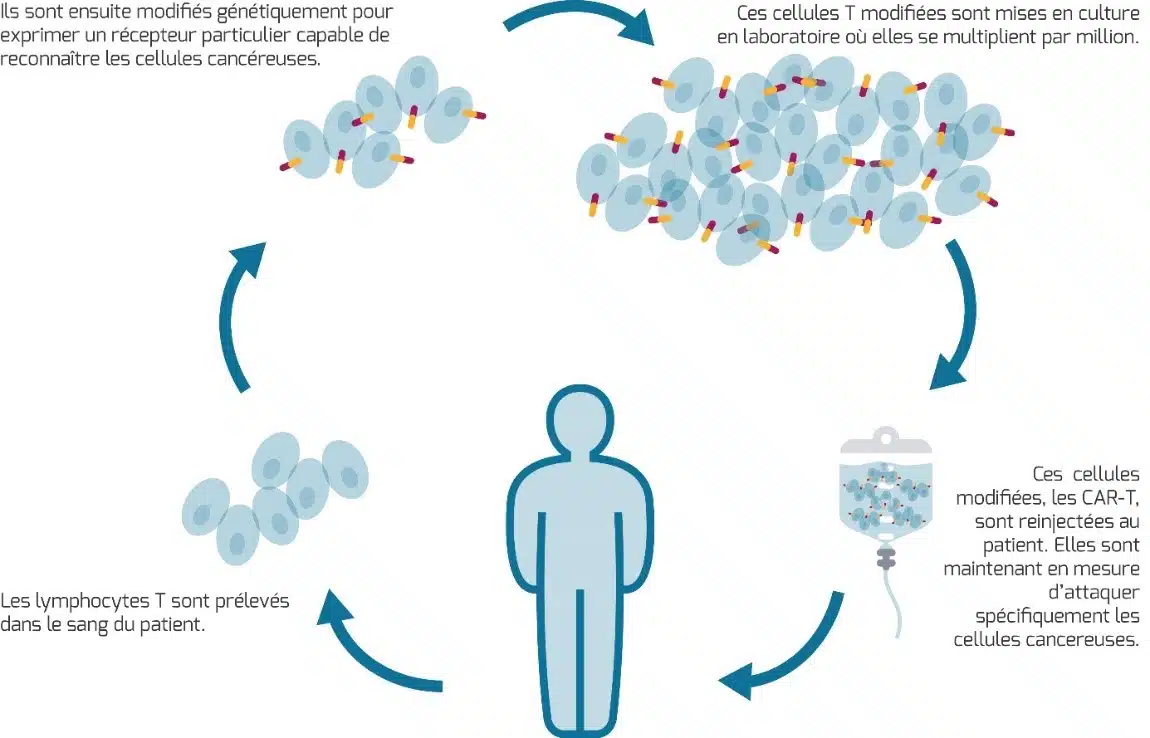
Le traitement par CAR-T cells (Chimeric Antigenic Receptor – T) ou cellules CAR-T est une thérapie cellulaire génétiquement modifiée (appelée également thérapie génique) qui vise à combattre le cancer en s’appuyant sur le propre système immunitaire du patient. Cette immunothérapie repose sur les lymphocytes T, des globules blancs dont le rôle est d’identifier et détruire toute cellule anormale ou infectée par des organismes étrangers (cellules cancéreuses, bactéries, virus).
Étape 1 : Prélèvement des lymphocytes T
La production des CAR-T cells commence par le prélèvement des lymphocytes T du patient qui sont ensuite modifiés génétiquement afin qu’ils puissent reconnaître les cellules cancéreuses. Pour cela, ils sont dans un premier temps collectés par leucaphérèse, un prélèvement sanguin ciblant les globules blancs.
Étape 2 : Fabrication des CAR-T cells
Après contrôle de leur qualité, ils sont modifiés génétiquement en laboratoire pour exprimer des récepteurs spécifiques à leur surface. On parle de récepteur antigénique chimérique (chimeric antigen receptor), CAR en anglais. Ces récepteurs permettront aux cellules modifiées, alors appelées CAR-T, de repérer des antigènes présents sur les cellules tumorales.
Étape 3 : Multiplication des CAR-T cells
Une fois créées, les CAR-T cells sont multipliées dans l’optique d’être administrées au patient.
Étape 4 : Administration des CAR-T cells
Avant l’injection, le patient reçoit une chimiothérapie lymphodéplétive dans le but d’affaiblir son système de défense immunitaire. Ainsi, en éliminant une partie des lymphocytes naturels, la multiplication des CAR-T cells sera favorisée et le risque de rejet sera limité. Une fois dans l’organisme, les CAR-T cells vont donc reconnaître et cibler les cellules tumorales de manière spécifique grâce au récepteur CAR, puis s’activer contre elles et les éliminer.
> En savoir plus sur l’immunothérapie via le site internet de INCa